业务咨询

![]() 发布时间:2025-08-29
发布时间:2025-08-29
![]() 环特生物
环特生物
![]() 浏览次数:449
浏览次数:449

编者按
自闭症,又称为孤独症谱系障碍(autism spectrum disorder, ASD),是一种以社交沟通缺陷、重复刻板行为等为特征的神经发育障碍疾病。你是否知道,超过半数的自闭症患者饱受胃肠道问题困扰?便秘、腹泻、腹痛等症状为何会如此频繁地与自闭症同时出现?数十年来,这个问题的答案一直隐藏在迷雾中。
3月6日,加州大学旧金山分校研究团队在Nature Communications发表最新研究,基于基因编辑技术,通过斑马鱼与爪蟾模型相互印证,首次系统性将ASD基因、肠神经系统(ENS)发育、胃肠道(GI)功能障碍联系起来,揭示了自闭症基因变异如何导致肠道神经系统发育异常,证实了肠神经元迁移障碍是潜在的机制,为理解ASD相关胃肠道问题提供了新的分子和细胞层面的见解,并指明了潜在的治疗靶点。
本研究中,研究人员基于基因编辑技术,在斑马鱼研究(斑马鱼基因编辑技术“解码”自闭症,助力神经科学研究!)的基础上,又使用爪蟾模型进一步验证了多种自闭症基因共同导致肠道神经元迁移障碍,证明了不同模式生物在揭示疾病机制方面的互补性和一致性,揭示了自闭症与胃肠道问题共病的分子机制,并提出了潜在的治疗策略。
01、研究亮点
• 已有研究表明,在斑马鱼中敲除CHD8基因,会导致肠神经元向肠道的定植减少和肠道运动功能障碍,且自闭症基因在人类肠神经元中表达富集。本研究基于基因编辑技术,利用爪蟾模型进一步验证,发现ASD基因变异会导致肠道神经元前体细胞(ENCCs)迁移缺陷;
• 首次系统地揭示了自闭症基因变异通过影响肠道神经系统发育而导致胃肠道问题的机制,证实了hcASD基因变异与胃肠道运动功能障碍的关联;
• 筛选了8种FDA批准的血清素相关药物,发现SSRI类药escitalopram和 5-HT6受体激动剂WAY-181187可显著改善DYRK1抑制引起的肠道动力障碍,揭示了增强血清素信号可能是治疗ASD相关GI问题的有效策略。
02、主要研究成果
1. 携带hcASD基因变异的患者普遍存在胃肠道运动功能障碍
研究人员分析了人类胚胎期肠道单细胞RNA测序数据,发现252个高置信度自闭症风险基因(hcASD基因)均显著富集表达。结果显示,相比于其他细胞类型,肠道神经元前体细胞(ENCCs)和肠神经元中的hcASD基因,其表达富集程度显著更高(p<0.0001),表明这些基因可能参与ENS的发育和功能调控。
随后,又利用数据库对携带16种hcASD基因致病变异的患者进行了分析,验证了GI症状与ASD基因变异相关,确认了ASD基因变异与GI功能障碍的强烈关联。数据结果显示,携带hcASD基因变异的16种基因变异患者中,51.7%有GI症状,而未受影响的对照组中,此类症状极少,平均患病率仅0.4%。超过80%的有GI症状诊断,且超过60%的患者存在GI运动功能障碍,尤其是便秘。
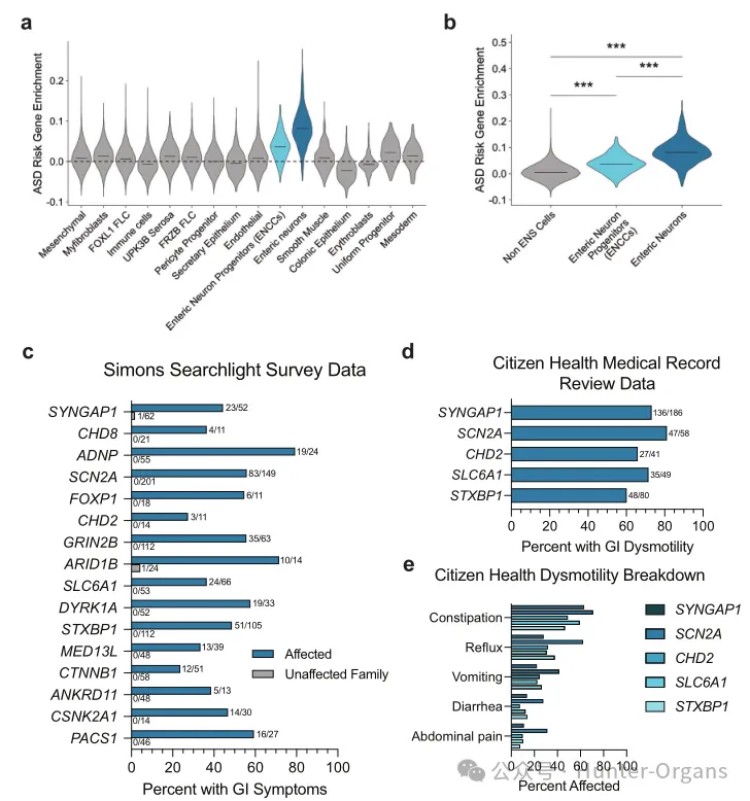
2. 体内动物实验揭示hcASD基因变异导致肠神经来源细胞迁移缺陷
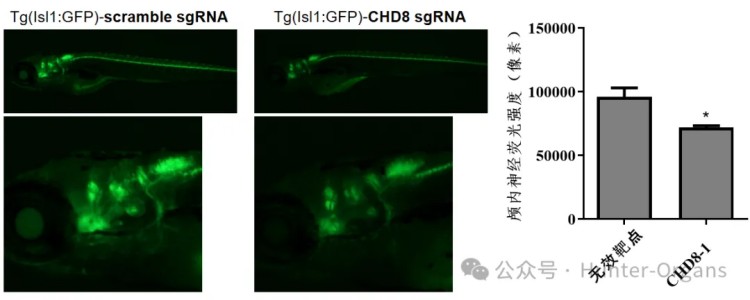
早期研究证据已表明,在斑马鱼中敲除CHD8基因(斑马鱼基因编辑技术“解码”自闭症,助力神经科学研究),会导致肠神经元向肠道的定植减少和肠道运动功能障碍;自闭症基因在成人人类肠神经元中表达富集。本研究中,利用热带爪蟾模型,基于基因编辑技术靶向了5个功能各异的hcASD基因——SYNGAP1、CHD8、SCN2A、CHD2、DYRK1A等,来比较突变组与对照组的肠神经来源细胞(ENCCs)迁移面积,做了进一步验证。
结果发现,尽管5个突变基因参与不同的细胞过程,如神经传递、染色质调节和激酶活性等,但它们均导致肠道神经元前体细胞(ENCCs)迁移面积显著减少,表明这些基因在ENS发育中具有收敛性功能,hcASD基因变异在体内破坏了肠神经来源细胞(ENCCs)的迁移,也进一步证明了不同模式生物在揭示疾病机制方面的互补性和一致性。
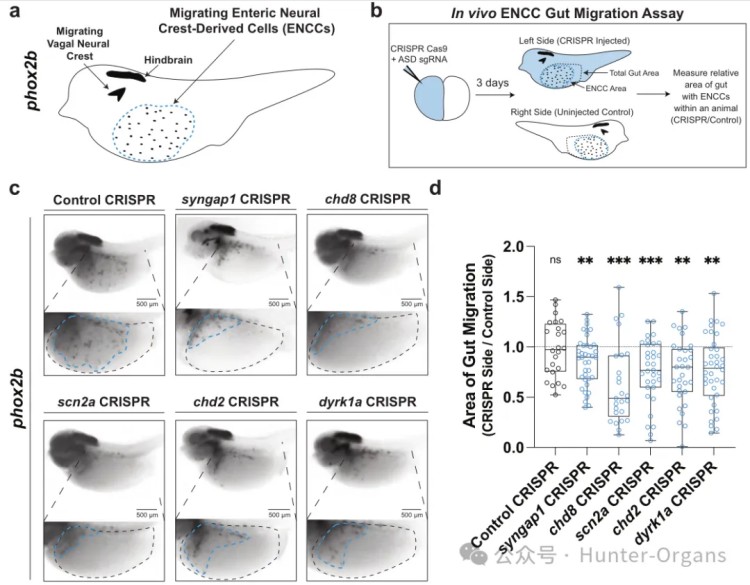
3. DYRK1A基因影响ENCCs迁移及早期神经嵴发育,并会导致肠道动力障碍
接着,研究人员利用基因编辑技术和Morpholino寡核苷酸(MO)分别敲低DYRK1A,均观察到ENCCs迁移减少,表明DYRK1A的功能缺失导致ENCCs迁移缺陷。进一步观察早期神经嵴标记物sox10的表达,发现Dyrk1a敲低导致早期神经嵴标记物sox10表达缺陷,CHD8、CHD2等其他hcASD基因也影响sox10,而SYNGAP1和SCN2A影响较小,因此,DYRK1A基因不仅影响早期神经嵴发育,也可能对后续的ENCC迁移有独立作用。使用条件性药物抑制策略,揭示了DYRK1A基因在ENCCs迁移过程中,具有独立于早期神经嵴发育的功能。
为了进一步评估发育过程中抑制DYRK1a是否会影响体内肠道运动,研究人员建立了体内肠道动力检测方法——荧光珠排泄实验,实验结果显示,与DMSO对照组相比,TG003处理组排出的荧光微珠数量显著减少(p=0.009),这表明,发育过程中抑制DYRK1a会出现肠阻样表现,肠道排泄显著减少,导致肠道动力障碍。
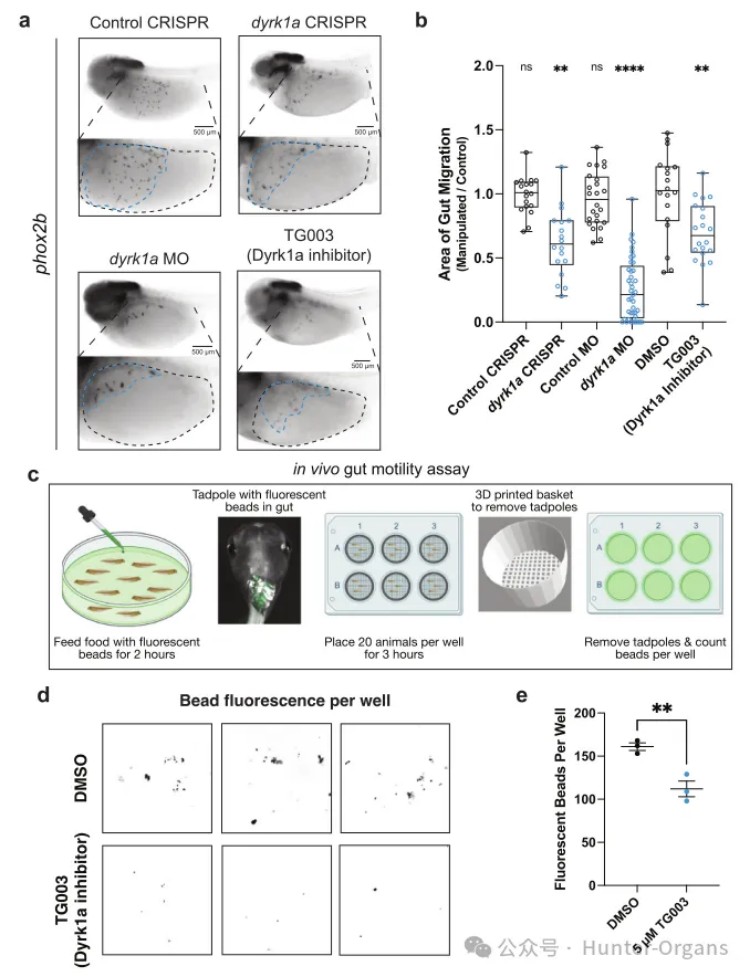
4. 血清素信号通路可缓解DYRK1A抑制引起的肠道运动障碍
已有研究表明,血清素(5-羟色胺,5-HT)是一种重要的小分子单胺,在中枢和外周神经系统中发挥多种生理功能,包括心脏收缩、肠蠕动、血管收缩等。本研究中,研究人员筛选了8种FDA批准的、影响血清素通路的药物,发现选择性5-羟色胺再摄取抑制剂(SSRI)类抗抑郁药物escitalopram(依他普仑)和5-HT6受体激动剂WAY-181187,可显著改善DYRK1抑制引起的肠道动力障碍。
这表明,DYRK1A相关的肠道功能障碍,可以通过急性治疗激活血清素信号通路来改善。
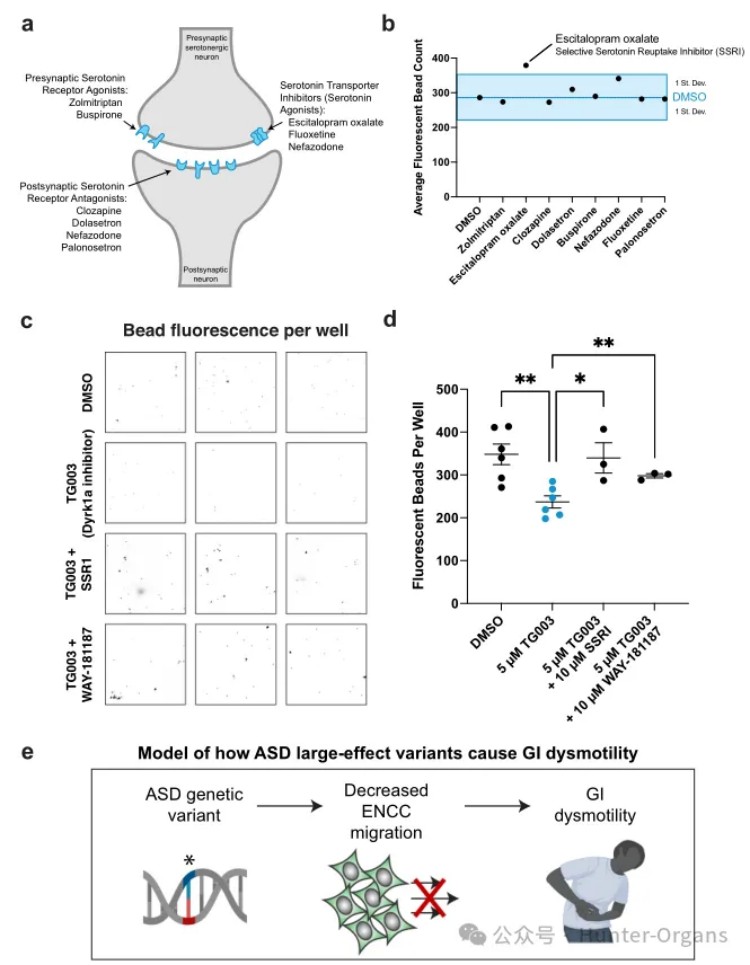
利用基因编辑技术,通过构建CHD8基因敲除嵌合体的斑马鱼自闭症模型,可以模拟人类CHD8突变相关自闭症的多种核心特征,如显著的行为抑制、社交障碍、胃肠道问题等。为了更好地助力自闭症等疾病研究,环特生物依托国际领先的斑马鱼、类器官、哺乳动物、人体临床等多维生物技术服务平台,构建了自闭症、抑郁症、焦虑症等200多种疾病模型,助您揭开神经科学研究的新篇章!欢迎新老客户咨询!
03、编者点评
本研究证实了hcASD基因变异与GI运动功能障碍之间的关联,并揭示了肠神经元迁移障碍是潜在的机制。五种功能不同的hcASD基因在体内实验中,均表现出对肠神经嵴来源细胞 (ENCC)迁移的破坏作用。DYRK1A研究表明,血清素信号通路的激活可能是一种有前景的治疗策略,用于改善 ASD 患者的 GI运动功能障碍,为理解 ASD 相关 G|问题提供了新的分子和细胞层面的见解,并指明了潜在的治疗靶点。
作为健康美丽产业CRO服务开拓者与引领者、斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、基因编辑、类器官、哺乳动物、人体”等多维生物技术服务体系,开展健康美丽CRO服务、科研服务、智慧实验室搭建三大业务。目前,环特已建立200多种斑马鱼模型,脑类器官、胃癌、心脏类器官及各种肿瘤类器官培养平台,欢迎有需要的读者垂询!
参考文献:
McCluskey, K.E., Stovell, K.M., Law, K. et al. Autism gene variants disrupt enteric neuron migration and cause gastrointestinal dysmotility. Nat Commun 16, 2238 (2025). DOI: 10.1038/s41467-025-57342-3