业务咨询

![]() 发布时间:2025-09-29
发布时间:2025-09-29
![]() 环特生物
环特生物
![]() 浏览次数:3
浏览次数:3

编者按
在糖尿病研究领域,细胞疗法可以促进胰岛β细胞的增殖与再生,从而恢复胰岛素的内源合成,但如何实现胰岛β细胞的功能性再生一直是科学家们努力攻克的难题。斑马鱼作为研究器官发育和组织再生的重要模型,在胰腺发育、胰岛素诱导β细胞和糖尿病研究中具有显著的优势。
本期,我们分享2024年10月发表在《Trends in Molecular Medicine》(IF=13.8)上的一项研究成果,该研究详细阐述了斑马鱼胰腺发育、β细胞再生的最新进展,及斑马鱼在糖尿病基因功能、疾病机制研究和治疗靶点等领域展现出的巨大价值,为胰岛β细胞和糖尿病治疗提供了新思路。
本研究中,通过结合基因编辑技术、高通量筛选等方法,在斑马鱼胰岛细胞发育(模型一览丨斑马鱼急性胰腺炎模型)中,研究人员创新性地提出了“四波模型”,即在斑马鱼发育的不同时相,胰岛细胞分别从4种细胞来源分化而来,为理解胰岛细胞的复杂发育过程提供了新视角。
01、研究亮点
基于单细胞转录组学和谱系追踪,发现sst1.1⁺细胞和krt4⁺细胞分化是斑马鱼胰岛素产生细胞再生的主要来源;
大规模体内小分子筛选已成功应用于斑马鱼,以无偏倚方法鉴定促进β细胞再生和葡萄糖控制的化合物。多种化合物已被证实在哺乳动物中能促进β细胞增殖、分化等;
斑马鱼活体成像可以在单细胞分辨率下,可视化观察复杂的生物学过程,如β细胞内的钙通量,以及胰岛的神经支配和免疫细胞行为;
在全基因组关联研究(GWAS)和单细胞测序等人类遗传数据中发现的基因功能,可以在斑马鱼中高效阐明。
02、主要研究成果
1. 斑马鱼胰腺特征
与哺乳动物胰腺类似,斑马鱼胰腺主要由外分泌细胞和内分泌细胞组成。胰岛内有几种内分泌细胞类型,包括分泌胰岛素的β细胞、分泌胰高血糖素的α细胞等,这些内分泌细胞聚集在一起,构成了精细组织结构——胰腺小体。
斑马鱼胰腺是一个高度血管化的器官,有大量的血管内皮细胞、平滑肌细胞和周细胞,受到外周神经元的支配,胰岛血管系统对维持全身葡萄糖稳态至关重要。
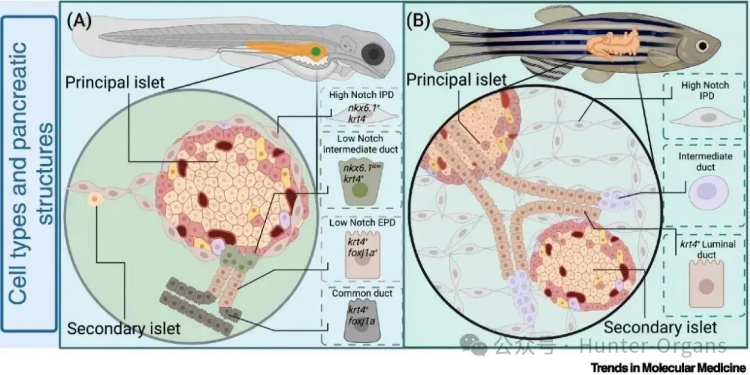
图1
2. 斑马鱼胰腺发育与次级胰岛的形成
两个胰腺原基及其融合形成了包含一个主要胰岛的胰腺。斑马鱼胰腺由背侧芽和腹侧芽融合形成,其中,背芽主要形成位于胰腺头部的大主胰岛中的内分泌细胞,腹芽则贡献外分泌细胞和部分内分泌细胞。研究表明,nkx6.1⁺细胞在早期阶段为多能前体细胞,随后逐渐发育为双潜能性导管前体细胞(tp1⁺ IPD),能够持续分化为内分泌细胞,并参与次级胰岛形成。
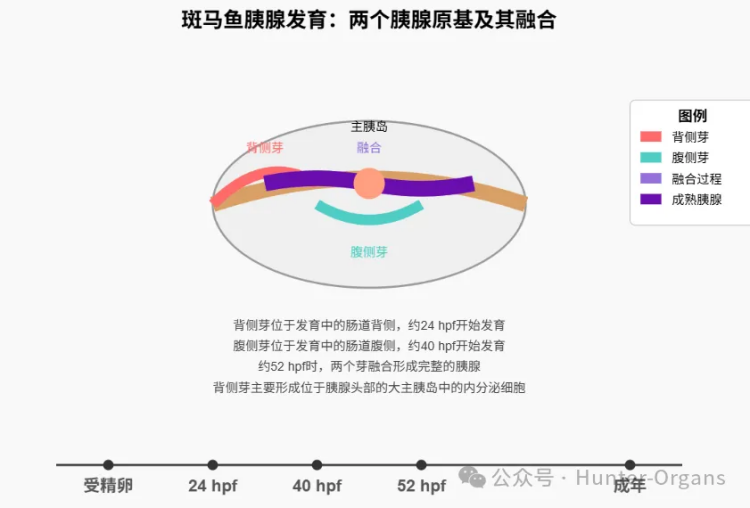
图2
3. 斑马鱼β细胞成熟
胰岛素分泌细胞的成熟过程对葡萄糖稳态至关重要,β细胞功能成熟,即获得了对葡萄糖的胰岛素分泌能力。研究表明,甲状腺激素是β细胞成熟的关键因子,可以激活β细胞中重要的转录调控。
Wnt4和Adjudin等分子可以促进β细胞功能成熟。斑马鱼筛选中发现的小分子,可增加胰岛素启动子活性、胰岛素mRNA 表达,并降低β细胞消融斑马鱼的血糖水平。转基因斑马鱼实验显示,Adjudin通过增加细胞钙反应和具有钙反应的β细胞百分比来促进β细胞的功能成熟。组蛋白去乙酰化酶(HDAC)抑制剂HC toxin最初在斑马鱼筛选中被发现能刺激pdx1表达,也能增强人iPSC来源的β细胞中功能性β细胞标志物表达增加,改善人和小鼠胰岛的葡萄糖刺激胰岛素分泌功能。
4. 斑马鱼β细胞的再生与增殖
斑马鱼作为重要的再生模型,相比于哺乳动物,其具有终生的胰岛素分泌细胞生成潜能。斑马鱼β细胞再生主要通过三种途径,分别为:
(1)β细胞自我增殖:受营养、ROS、衰老和免疫状态调控,通过现有β细胞的自我复制来增加β细胞数量;
(2)其他胰腺细胞转分化:在特定条件下,将其他胰腺细胞类型,如α细胞、δ细胞,尤其是sst1.1⁺ δ细胞、ε细胞和腺泡细胞等直接重编程,转分化为β细胞;
(3)导管来源的β细胞新生:由胰管细胞分化产生新的β细胞,如Notch信号调控的导管细胞(tp1⁺ IPD)是β细胞新生的主要来源;CDK5抑制剂、叶酸等小分子可促进导管向β细胞分化。

图3
随后,研究人员在STZ模型、MTZ模型、部分胰切除模型这三种β细胞损伤模型中验证了成年斑马鱼的细胞增殖状态。在STZ模型中,消融后7天内很少发现β细胞增殖,但可在导管上皮中识别出再生性β细胞。2 周后,胰岛中出现大量散在的Pcna+细胞。MTZ模型中,胰岛和导管上皮中观察到许多Pdx1+分裂细胞。2周后,Pcna+细胞主要位于胰岛外,胰岛内的增殖状态与对照组相当;而在部分胰切除模型中,则可以观察到更明显的β细胞增殖。这表明,不同的损伤模型可以刺激不同的再生性细胞反应。
5. 斑马鱼胰腺发育中的转录和表观遗传调控
内胚层器官细胞的发育依赖于一系列在连续阶段发生的协调转录调控事件。sox9b、pax6b、neurod1等多种转录因子,是胰岛前体细胞生成的重要分子遗传学事件,在胰腺发育中发挥关键作用。其中,ascl1b和neurod1,被认为共同担负了哺乳动物Neurog3的类似的作用。
表观遗传修饰是胰腺和胰岛细胞发育的关键调节因子。hdac1、dnmt1等表观调控因子影响胰腺发育与再生能力。 值得一提的是,Dnmt1缺失可增强 NTR/MTZ 模型中胰岛素产生细胞的恢复,表明表观遗传重编程是β细胞再生的关键药物靶点。
6. 微环境对胰腺血管与神经支配的作用
胰腺血管系统和神经支配对胰岛结构和功能有重要的影响。外周自主神经和感觉神经与胰岛紧密连接,然后迁移出去。特异性消融这些神经元可以部分抑制其他神经元从胰岛迁移,最终导致胰岛神经支配减少。
研究表明,神经元与内分泌细胞之间存在功能耦合,δ细胞可能作为“枢纽”协调胰岛活动。所有内分泌细胞都与外周神经元相连,急性或慢性方式消除神经元活动均可显著降低β-β和 α-β活动耦合。一小部分具有可检测的胰岛周围神经活动耦合的δ细胞显示出比其对应物更高的同类型耦合活性,表明一些接收来自外周神经输入的δ细胞充当协调S细胞活动的枢纽。这种功能模式似乎是保守的,类似于β细胞。
7. 导管重塑与内分泌发生耦合
研究人员提出“四波内分泌发生模型”,强调导管重塑与内分泌细胞分化是协同过程。“四波模型”,即胰岛细胞在斑马鱼发育的不同时期,可以分别从4种细胞来源分化而来——
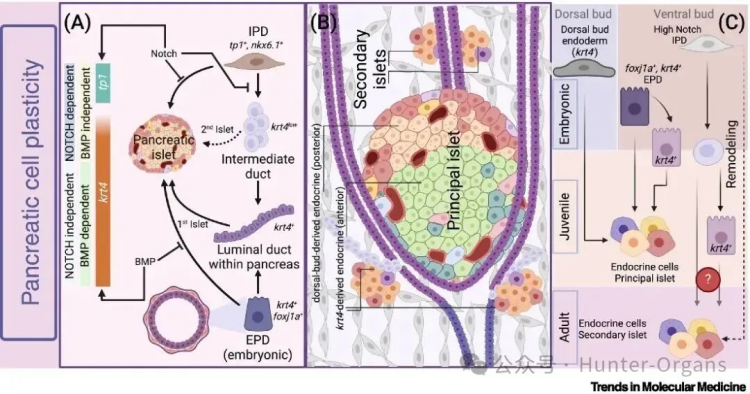
图4
第一波:早期胚胎阶段的内分泌细胞直接分化:在斑马鱼胚胎发育的早期阶段,背侧芽孢的内胚层上皮可以直接分化为内分泌细胞。这些细胞最终分布在主胰岛的后部,构成了胰岛细胞发生的第一波。
第二波:krt4+导管细胞的分化:在受精后56至72hpf期间,krt4+细胞可以标记胰腺外部的导管(EPD)和中间导管细胞,部分导管上皮细胞可以想向内分泌细胞分化,构成了胰岛细胞发生的第二波。krt4⁺导管细胞在青少年期通过重塑形成新的内分泌细胞。
第三波:幼年阶段的内分泌细胞分化:在斑马鱼进入幼年阶段,内分泌细胞的发生并未停止。krt4+的EPD逐渐向胰腺内部延伸,其中部分选择性分化为内分泌细胞,并逐渐追加到主胰岛的前方。这个过程在斑马鱼发育的幼年阶段极为显著,构成了胰岛细胞发生的第三波。
第四波:tp1+ IPD细胞的重塑与分化:在后期发育阶段,tp1+的Notch反应性胰腺内导管(IPD)细胞(krt4-)经历导管重塑,部分细胞分化形成次级胰岛,而剩余的导管上皮则逐渐聚集,并排列成具有管腔样结构的krt4+的胰腺主/次级胰管。IPD上皮细胞的命运决定,与导管上皮细胞重塑与内分泌细胞的发生紧密相关;而新生的胰岛细胞是胰腺体尾部的次级胰岛内分泌细胞的主要来源,构成了胰岛细胞发生的第四波。

近年来,斑马鱼模型凭借其与人类高度保守的胰腺结构与功能,胚胎通体透明的可视化等特性,为胰腺炎及相关病理机制研究、药物筛选提供了新方法。环特生物依托国际领先的斑马鱼、类器官、哺乳动物、人体临床等多维生物技术服务平台,开发了高效的斑马鱼胰腺炎模型,并利用该模型系统评价产品改善胰腺炎功效,为开发新型胰腺炎治疗策略提供强大的临床前评价工具和科学证据。详情请点击:模型一览丨斑马鱼急性胰腺炎模型
03、编者点评
斑马鱼作为一种模型生物,在研究胰岛β细胞的发育、功能和再生中扮演着越来越重要的角色。通过结合最新的基因编辑技术、高精度测序和高通量筛选方法,深入理解斑马鱼胰岛β细胞在发育和再生过程中的命运决定的理解,为糖尿病细胞替代治疗提供了新的策略和希望。
作为健康美丽产业CRO服务开拓者与引领者、斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、基因编辑、类器官、哺乳动物、人体”等多维生物技术服务体系,开展健康美丽CRO服务、科研服务、智慧实验室搭建三大业务。目前,环特已建立200多种斑马鱼模型,脑类器官、胃癌、心脏类器官及各种肿瘤类器官培养平台,欢迎有需要的读者垂询!
参考文献:
Jiarui Mi, Lipeng Ren et al. Leveraging zebrafish to investigate pancreatic development, regeneration, and diabetes. Trends Mol Med.October 2024, Vol. 30, No. 10,DOI: 10.1016/j.molmed.2024.05.002