业务咨询

![]() 发布时间:2023-04-06
发布时间:2023-04-06
![]() 环特生物
环特生物
![]() 浏览次数:6140
浏览次数:6140

非酒精性脂肪性肝病(NAFLD)是全球慢性肝病的主要原因,然而,目前还没有治疗方法或药物能够阻止或逆转脂肪肝。随着病情的进展,患者会出现不可逆肝损伤,甚至可能需要肝移植。由于缺乏研究模型,NAFLD防治方法的研究面临很大挑战。
今天我们特别关注一篇在NAFLD领域的最新研究成果——《Engineered human hepatocyte organoids enable CRISPR-based target discovery and drug screening for steatosis》,该研究团队通过多种技术手段构建了NAFLD类器官模型来研究NAFLD进展的不同因素,并且成功发现FADS2基因是一个新的与NAFLD相关的关键基因,为后续治疗提供了一个新的起点。
一、研究背景
全球约有1/4的人口深受非酒精性脂肪性肝病(NAFLD)影响[1]。NAFLD是一种进行性疾病。从肝脏内脂肪堆积开始,即肝脏脂肪变性,可发展为非酒精性脂肪性肝炎(NASH),最终导致肝衰竭或癌症[2,3]。尽管NAFLD的患病率很高,并且还在不断上升,但任何阶段的NAFLD都缺乏有效的药物治疗[4,5]。
在已有的研究中,NAFLD生物学和假定的药物治疗主要以啮齿类动物为模型进行研究[6]。但固有的物种间差异,削弱了研究结果与人体的对应性。依赖原代细胞或多能干细胞衍生细胞的相关体外人NAFLD模型已经出现[7-9],但其对高通量药物筛选的适用性仍未得到证实。本文使用人胎儿肝细胞构建类器官模型,在此模型的基础上建立了基于CRISPR的筛选平台,称为FatTracer,并且成功筛选到关键的靶点FADS2基因,有助于更好的了解以及治疗NAFLD。
二、主要研究结果
1. 建立类器官疾病模型模拟不同机制的脂肪变性
构建三种不同肝脏类器官以模拟不同的脂肪变性触发因素,分别是:(1)游离脂肪酸(FFA)诱导的脂肪变性类器官模型,用以研究饮食导致的脂肪变性;(2)编辑PNPLA3基因诱导的个体遗传敏感性类器官模型,用以研究个体遗传敏感性差异导致的脂肪变性;(3)编辑APOB或MTTP基因诱导的脂质代谢障碍类器官模型,用以研究脂质代谢障碍所致的脂肪变性。
(1)添加低浓度的FFA(<80 µM),类器官能够正常代谢,不会形成甘油三酯沉积,添加较高浓度FFA(>80 µM),类器官中出现甘油三酯积累,提示出现脂肪变性。最高浓度FFA添加后(640 µM),统计类器官的脂肪变性比率约40%,且类器官的增殖能力受损;
(2)PNPLA3基因中编码I148M变异的rs738409变异是已见报道的与NAFLD相关性最强的遗传风险因素[10]。作者利用CRISPR方法在类器官中引入I148M变体,生成杂合子(PNPLA3WT/I148M)和纯合子(PNPLA3I148M/I148M)变体类器官,同时使用引入空载体但未编辑的类器官(PNPLA3WT)作为内部对照,还对PNPLA3进行了敲除(PNPLA3−/−)。 PNPLA3WT类器官在标准培养条件下不会出现脂肪沉积。但是三个编辑过PNPLA3基因型的类器官都自发产生了脂肪沉积。PNPLA3−/−类器官积累脂肪最多(约8%脂肪变性),其次是I148M纯合子类器官(约5%)和杂合子I148M类器官(约2%);
(3)建立两种易导致NAFLD的单基因脂质疾病模型:家族性低β脂蛋白血症和无β脂蛋白血症。这些疾病最常见的原因单等位基因或更罕见的双等位基因缺失(家族性低β脂蛋白血症缺失APOB,无β脂蛋白血症缺失MTTP),由此产生的极低密度脂蛋白(VLDL)分泌受损,反过来又会导致脂肪变性。作者首先证实野生型类器官主动分泌VLDL颗粒,从而不会积累起甘油三酯。然后,作者对野生型类器官进行基因编辑,构建了APOB和MTTP双等位基因缺失的类器官模型,通过脂质含量的定量、葡萄糖同位素示踪实验,表明由于糖源性脂肪的积累,肝脏类器官自发出现脂肪沉积,导致脂肪变性,成功构建了遗传性脂肪变性肝脏类器官。
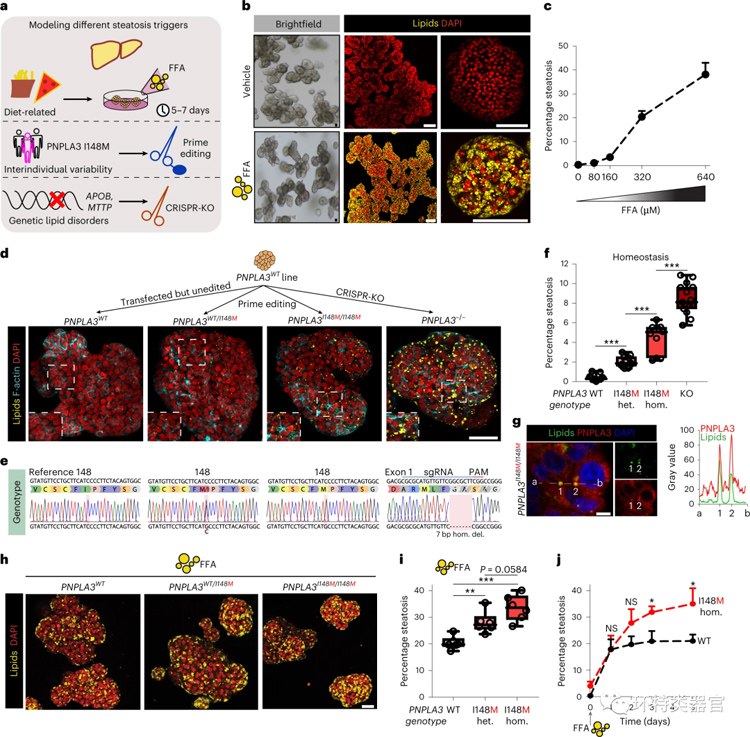
图1 构建不同机制的肝脏类器官模型
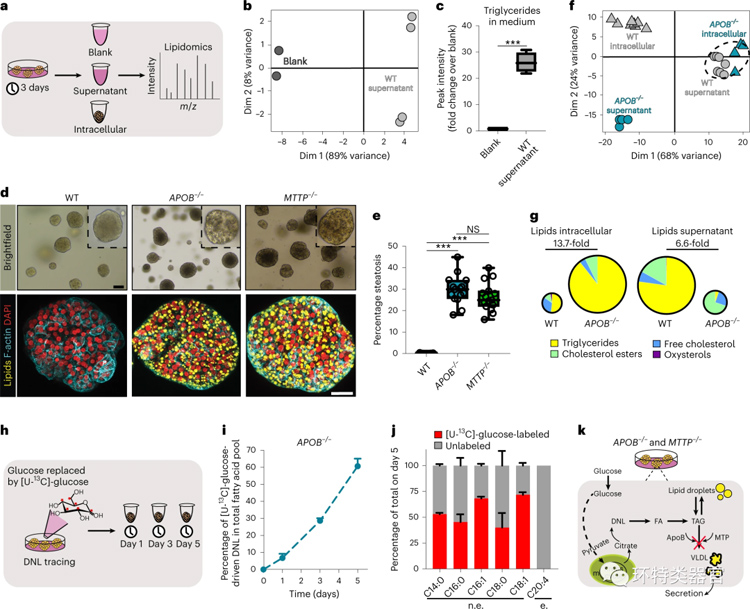
图2 建立脂质代谢障碍类器官模型并探究机制
2. 筛选通过减少脂肪变性治疗NAFLD的药物
上述开发的模型可以搭建药物筛选平台,以识别直接作用于肝细胞以减少脂肪变性、治疗NAFLD的药物。作者将FFA诱导的模型和脂质代谢障碍模型暴露在多种候选药物中,通过尼罗红染色评估脂肪沉积,开发出脂滴评分系统来评价药物有效性。并对遗传易感性模型添加FFA,诱导饮食导致的脂肪变性模型,再利用筛选出的几种有治疗效果的药物进行治疗,发现治疗效果在遗传敏感性模型上被削弱。
研究还在整个转录组水平上研究了药物反应和作用,以评估药物机制和整体细胞反应(包括不良反应),RNA-seq显示,在可以同等减少脂肪变性的所有不同药物的处理下,差异基因表达分析存在明显差异。实验结果显示,对NAFLD有效的药物通过一个共同的机制起作用,即阻止糖生成脂类。该研究还观察到,NAFLD高风险突变的类器官(PNPLA3I148M/I148M)与没有突变的类器官(PNPLA3WT)对所有药物的应答方式不同,这表明类器官可以作为个性化医疗的工具。
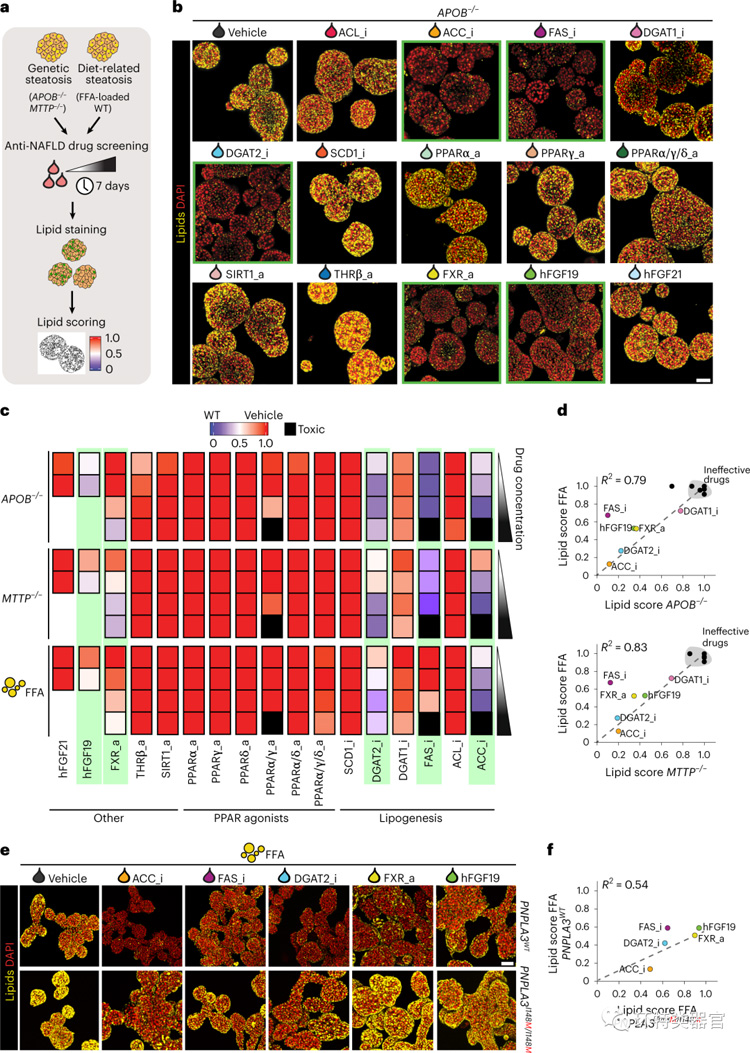
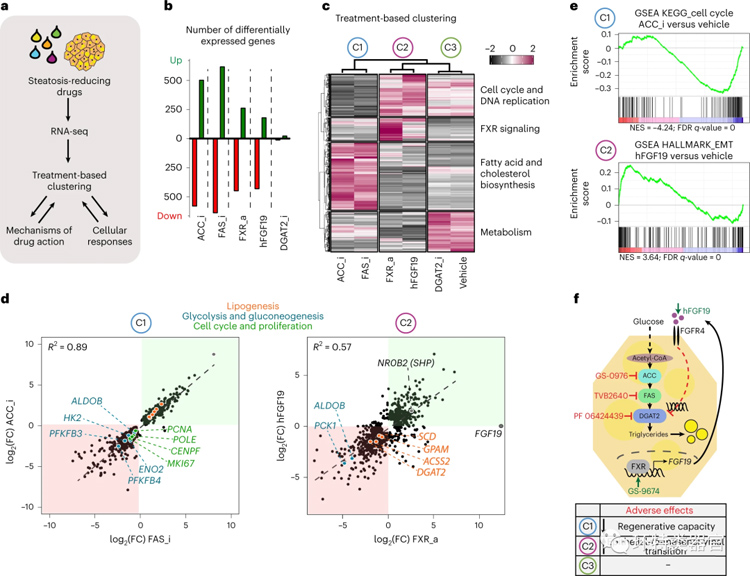
图3 基于类器官模型的药物筛选
3. 建立FatTracer平台
研究人员利用突变体,对潜在的脂肪变性调节剂和可能的药物靶点进行基于CRISPR的遗传筛选,并将这个平台命名为FatTracer。受到药物筛选中出现的非常特定的靶点依赖性的启发,对35个与脂质代谢和NAFLD有关的候选基因进行了筛选,发现FADS2基因(编码脂肪酸去饱和酶2)是一个未见报道的、与NAFLD疾病相关的关键基因,FADS2基因的缺失使得类器官中的脂肪含量大大增加,FADS2过表达显著降低了脂肪沉积的程度。因此,FADS2表达水平的调节直接决定了肝细胞内脂肪变性的水平,无论是发展中的脂肪变性还是已经存在的脂肪变性,表明FADS2是治疗NAFLD的一个新的有效治疗靶点。
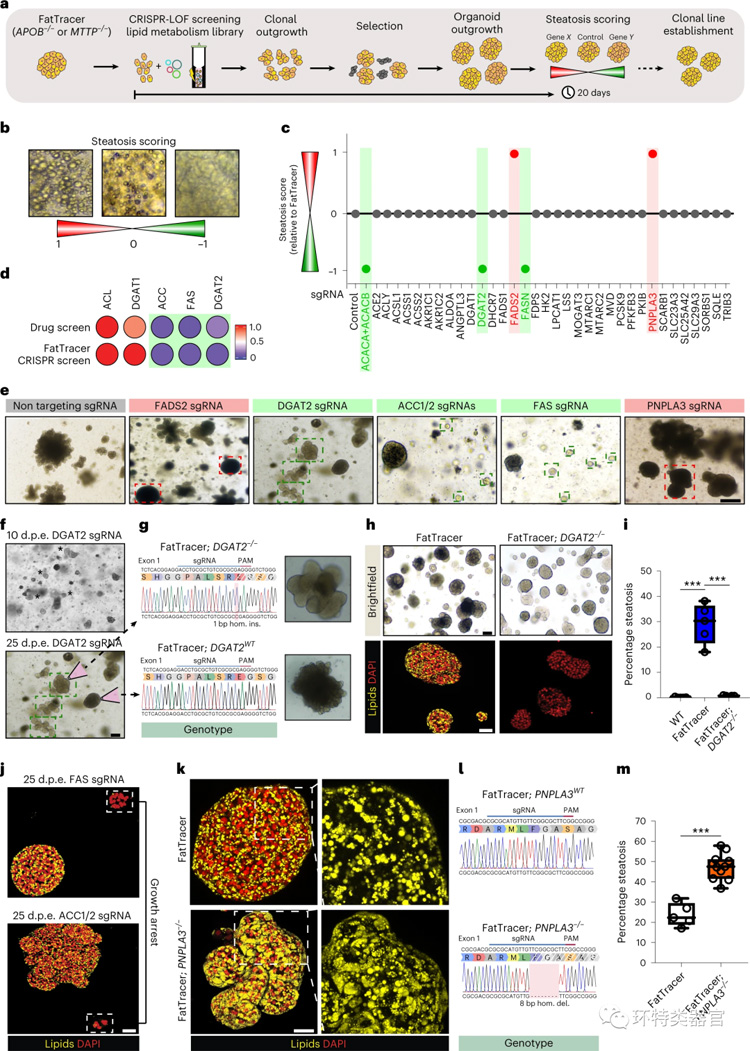
图4 FatTracer筛选平台
三、编者点评
这是一项非常先进的类器官研究,并且与深受NAFLD困扰的患者息息相关。本篇文章捕获了一个新的关键性基因FADS2,是治疗NAFLD的一个新的有效治疗靶点,可能会对这一种困扰世界1/4人口的疾病有突破性的进展。
此外,本文提供了一种类器官技术的运用新思路,即通过基因编辑构建非肿瘤疾病的类器官模型,用于毒理药理研究、功效评价等,丰富了体外模型的种类,并且可以解决动物模型与人体对应性不佳的问题。
作为斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、类器官、哺乳动物、人体”四位一体的综合技术服务体系,开展科研服务、智慧实验室建设和精准医疗三大业务。目前,环特类器官平台正致力于开发基于基因编辑技术的多种非肿瘤疾病的类器官模型,未来将为食品、药品、化妆品等行业提供更多精准评价与机制研究模型,敬请期待!
参考资料:
[1] Younossi ZM, Koenig AB, Abdelatif D, Fazel Y, Henry L, Wymer M. Global epidemiology of nonalcoholic fatty liver disease-Meta-analytic assessment of prevalence, incidence, and outcomes. Hepatology. 2016 Jul;64(1):73-84.
[2] Kneeman JM, Misdraji J, Corey KE. Secondary causes of nonalcoholic fatty liver disease. Therap Adv Gastroenterol. 2012 May;5(3):199-207.
[3] Liebe R, Esposito I, Bock HH, Vom Dahl S, Stindt J, Baumann U, Luedde T, Keitel V. Diagnosis and management of secondary causes of steatohepatitis. J Hepatol. 2021 Jun;74(6):1455-1471.
[4] Younossi ZM. Non-alcoholic fatty liver disease - A global public health perspective. J Hepatol. 2019 Mar;70(3):531-544.
[5] Mullard A. FDA rejects NASH drug. Nat Rev Drug Discov. 2020 Aug;19(8):501.
[6] Ramli MNB, Lim YS, Koe CT, Demircioglu D, Tng W, Gonzales KAU, Tan CP, Szczerbinska I, Liang H, Soe EL, Lu Z, Ariyachet C, Yu KM, Koh SH, Yaw LP, Jumat NHB, Lim JSY, Wright G, Shabbir A, Dan YY, Ng HH, Chan YS. Human Pluripotent Stem Cell-Derived Organoids as Models of Liver Disease. Gastroenterology. 2020 Oct;159(4):1471-1486.e12.
[7] Collin de l'Hortet A, Takeishi K, Guzman-Lepe J, Morita K, Achreja A, Popovic B, Wang Y, Handa K, Mittal A, Meurs N, Zhu Z, Weinberg F, Salomon M, Fox IJ, Deng CX, Nagrath D, Soto-Gutierrez A. Generation of Human Fatty Livers Using Custom-Engineered Induced Pluripotent Stem Cells with Modifiable SIRT1 Metabolism. Cell Metab. 2019 Aug 6;30(2):385-401.e9.
[8] Ouchi R, Togo S, Kimura M, Shinozawa T, Koido M, Koike H, Thompson W, Karns RA, Mayhew CN, McGrath PS, McCauley HA, Zhang RR, Lewis K, Hakozaki S, Ferguson A, Saiki N, Yoneyama Y, Takeuchi I, Mabuchi Y, Akazawa C, Yoshikawa HY, Wells JM, Takebe T. Modeling Steatohepatitis in Humans with Pluripotent Stem Cell-Derived Organoids. Cell Metab. 2019 Aug 6;30(2):374-384.e6.
[9] Kozyra M, Johansson I, Nordling Å, Ullah S, Lauschke VM, Ingelman-Sundberg M. Human hepatic 3D spheroids as a model for steatosis and insulin resistance. Sci Rep. 2018 Sep 24;8(1):14297.
[10] Romeo S, Kozlitina J, Xing C, Pertsemlidis A, Cox D, Pennacchio LA, Boerwinkle E, Cohen JC, Hobbs HH. Genetic variation in PNPLA3 confers susceptibility to nonalcoholic fatty liver disease. Nat Genet. 2008 Dec;40(12):1461-5.