业务咨询

![]() 发布时间:2023-06-20
发布时间:2023-06-20
![]() 环特生物
环特生物
![]() 浏览次数:6498
浏览次数:6498

编者按
湖北大学生命科学学院院长张冬卉教授是环特生物院士专家工作站专家,长期致力于以人诱导性多能干细胞分化来源的心肌细胞等功能细胞为研究对象,通过开发新型技术方法,构建心肌微器官,并基于此研究心肌病致病机理,开发针对心肌梗死、心律失常、心衰的新型治疗方案。
今天,我们特别介绍一项张教授于2022年10月11日发表在《Cell Discovery》的近期研究——Generation of high-performance human cardiomyocytes and engineered heart tissues from extended pluripotent stem cells,该研究利用人扩展多能干细胞(EPSC)诱导出心肌细胞,并测试了这种新型来源的心肌细胞的性能,为心脏相关研究提供了新模型。
一、 研究背景
对于心脏疾病建模、药物筛选和细胞治疗而言,一个有效的体外模型至关重要,但供体人心肌细胞却非常稀缺,因此人胚胎干细胞(ESCs)和诱导性多能干细胞(iPSCs)诱导而来的心肌细胞被广泛用于心脏相关的研究[1,2]。然而,ESCs/iPSCs面临着异质性、存活率差、分化偏向性等挑战,限制了其应用[3,4]。为了解决这些问题,科研人员做了大量的工作,包括优化培养条件和获得更强大的、新的多能细胞类型[3]。2017年,邓宏魁团队构建出了人扩展多能干细胞(EPSCs),同时具有胚内和胚外组织的发育潜能[5],与ESCs/iPSCs来源的肝细胞相比,EPSCs来源的肝细胞显示出更好的功能,并且其转录组与人原代肝细胞的转录组更为相似[6]。
然而,EPSCs能否高效诱导生成其他谱系如心肌细胞,以及EPSCs来源的心肌细胞与ESCs/iPSC来源的心肌细胞相比如何发挥作用,目前尚未见研究。因此,本研究利用EPSCs诱导心肌细胞及心脏类器官,并将其与iPSCs诱导的心肌细胞及心脏类器官进行线粒体功能、钙离子流、收缩特性和挽救裸鼠心肌梗死模型方面的对比,观察其功能特性,研发新型心肌体外模型。
二、 研究成果
对于心脏疾病建模、药物筛选和细胞治疗而言,一个有效的体外模型至关重要,但供体人心肌细胞却非常稀缺,因此人胚胎干细胞(ESCs)和诱导性多能干细胞(iPSCs)诱导而来的心肌细胞被广泛用于心脏相关的研究[1,2]。
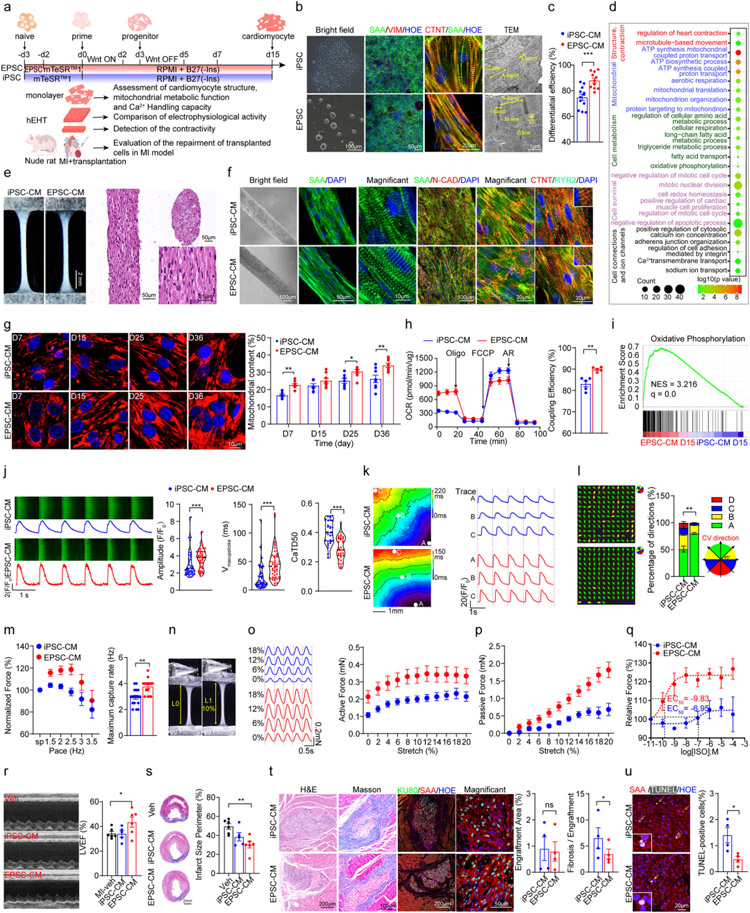
原文图1 EPSCs诱导的高性能心肌细胞及心脏类器官
本研究的整体实验流程如a图所示,直接将EPSCs按传统方法[1,7]进行心肌细胞的诱导会导致实验的失败,因此研究人员先将EPSCs的培养基从EPSCs特制培养基换为mTeSRTM 1(一种商品化的干细胞培养基)培养2天,可诱导生成心肌细胞(b图)。EPSCs可稳定、重复诱导产生心肌细胞,并且诱导效率显著高于iPSCs(c图),并且EPSCs诱导的高性能心肌细胞与iPSCs诱导的一样,也可搏动(视频1)。这些结果显示,EPSCs具有良好的向心肌细胞分化的潜能。
成功诱导心肌细胞后,研究人员将它们的结构、线粒体功能进行了对比。转录组GO分析显示,与iPSCs诱导的心肌细胞相比,EPSCs诱导的心肌细胞中肌小节排布和代谢成熟相关基因表达增强(d图)。这两种细胞组成的心脏类器官的肌小节结构无显著差异(e图),但EPSCs来源的心脏类器官具有更成熟的细胞结构,表现为N-Cadherin和RYR2标记的横小管的极化分布(f图)以及线粒体质量显著升高(g图)。利用Seahorse XF分析仪对两种来源的心肌细胞进行线粒体呼吸的监测,结果显示EPSCs诱导的心肌细胞具有更高的基线耦合效率(h图),并且转录组GSEA富集分析也显示,EPSCs诱导的心肌细胞中氧化磷酸化相关基因富集(i图)。综上,与iPSCs诱导的心肌细胞相比,EPSCs诱导的心肌细胞展现出更成熟的形态结构以及更完善的功能。
研究人员又进一步测试了两种来源细胞的钙离子流,结果显示,与iPSCs诱导的心肌细胞相比,EPSCs诱导的心肌细胞表现出更高的钙瞬变幅度和更短的钙离子衰减时间,表明钙循环相对快速和成熟(j图)。并且对两种来源细胞的电传导速度及传播方向进行对比后可见,虽然两者的传导速度(k图)相当,但EPSCs诱导的心肌细胞及心脏类器官具有更好的传播方向均匀性(l图)。并且,力传感器捕捉到的结果显示,EPSCs诱导的心脏类器官表现出正向起搏反应,在2.5 Hz时达到平均1.2倍的力(m图)。研究人员还评估了一下两种心脏类器官渐进性牵张(n图)以及异丙肾上腺素刺激时的正性肌力反应,结果显示,EPSCs诱导的心脏类器官在渐进性牵张中表现出更明显的正性(o图)和负性(p图)肌力反应。并且,与iPSCs诱导的心脏类器官相比,EPSCs诱导的心脏类器官对异丙肾上腺素的敏感性更大(q图)。
本文又为了研究EPSCs诱导的心肌细胞能否在体内的心肌中存活并改善缺血心脏损伤,研究人员将EPSCs和iPSCs诱导的心肌细胞肌肉注射至心肌梗死裸鼠模型的心肌上,结果表明,与未注射细胞的对照组相比,注射EPSCs诱导的心肌细胞6周后,心肌梗死裸鼠的左心室射血分数和左心室短轴缩短率显著改善(r图),并且梗死面积减小(s图),说明移植EPSCs诱导的心肌细胞有助于减轻心肌梗死裸鼠模型的心脏损伤。研究人员还发现,虽然两种来源的心肌细胞可形成大小相仿的移植物(t图),但EPSCs来源的移植物的纤维化程度较轻(t图)以及凋亡比例较低(u图)。这些结果说明,与iPSCs诱导的心肌细胞相比,移植EPSCs诱导的心肌细胞可能更有利于长期的心肌损伤修复。
三、 编者点评
1. 本文为心肌损伤修复等领域提供了一种新型的模型,为推动心肌相关疾病及基础研究作出了巨大贡献;
2. 这是一项新颖的研究,利用了一款新型的多能干细胞作为诱导心肌细胞的来源细胞,获得了一系列数据作为EPSCs诱导的心肌细胞下游应用的支持证据,非常详实,适合每一个想要利用这一模型的学者拜读。
3. 本文短小精悍,仅2页,本文还含有大量补充信息,在此不能全部展现,推荐各位读者移步原文仔细阅读。
作为斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、类器官、哺乳动物、人体”四位一体的综合技术服务体系,开展科研服务、智慧实验室建设和精准医疗三大业务。目前,环特类器官平台已经推出多能干细胞诱导的心肌细胞以及心脏类器官等模型,欢迎有需要的读者垂询!
参考资料:
[1] Lian, X. et al. Directed cardiomyocyte differentiation from human pluripotent stem cells by modulating Wnt/β-catenin signaling under fully defined conditions. Nat. Protoc. 8, 162–175 (2013).
[2] Gonzalez, R., Lee, J. W. & Schultz, P. G. Stepwise chemically induced cardiomyocyte specification of human embryonic stem cells. Angew. Chem. Int. Ed.Engl. 50, 11181–11185 (2011).
[3] Lund, R. J., Närvä, E. & Lahesmaa, R. Genetic and epigenetic stability of human pluripotent stem cells. Nat. Rev. Genet. 13, 732–744 (2012).
[4] Cahan, P. & Daley, G. Q. Origins and implications of pluripotent stem cell variability and heterogeneity. Nat. Rev. Mol. Cell Biol. 14, 357–368 (2013).
[5] Yang, Y. et al. Derivation of pluripotent stem cells with in vivo embryonic and extraembryonic potency. Cell 169, 243–257 (2017).
[6] Wang, Q. et al. Generation of human hepatocytes from extended pluripotent stem cells. Cell Res. 30, 810–813 (2020).
[7] Park, S. J. et al. Insights into the pathogenesis of catecholaminergic polymorphic ventricular tachycardia from engineered human heart tissue. Circulation 140, 390–404 (2019).