业务咨询

1、实验原理
细胞自噬是真核细胞中普遍存在的一种自我保护机制,细胞存在老化受损的细胞器、错误合成的蛋白质、入侵细胞的细菌以及大分子物质等,细胞自噬通过形成自噬体包裹这些对细胞有害的物质,并与溶酶体结合形成自噬溶酶体来分解、清除这些物质,保持细胞内环境稳态以及细胞内物质的循环利用。LC3-II和p62是细胞自噬途径中的两个关键蛋白,它们在自噬过程中发挥着重要的作用,分别参与自噬体的形成和自噬底物的识别与降解。在细胞质中,LC3主要以LC3-I的形式存在,当自噬被激活时,LC3-I会经过脂质化修饰,形成LC3-II。LC3-II能够识别并结合自噬体膜上的其他自噬相关蛋白(如ATG5-ATG12复合体),从而促进自噬体的成熟和与溶酶体的融合。p62(也称为SQSTM1)是一种多功能的蛋白质,它在细胞自噬过程中主要作为自噬底物的识别蛋白,p62能够识别并结合细胞内受损的蛋白质、蛋白质聚集体以及受损的细胞器等,它通过其泛素结合域(UBA)与泛素化的蛋白质相互作用,从而将这些需要降解的底物聚集在一起。LC3-II和p62在自噬过程中相互协作,p62通过其LIR结构域与LC3-II结合,将泛素化的底物连接到自噬体膜上,从而促进自噬体的形成和底物的降解,在自噬激活时,LC3-II的增加会促进p62的降解,从而减少细胞内p62的积累。
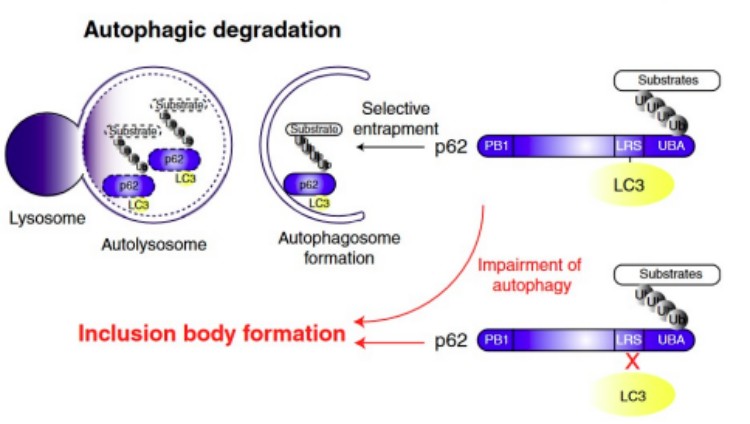
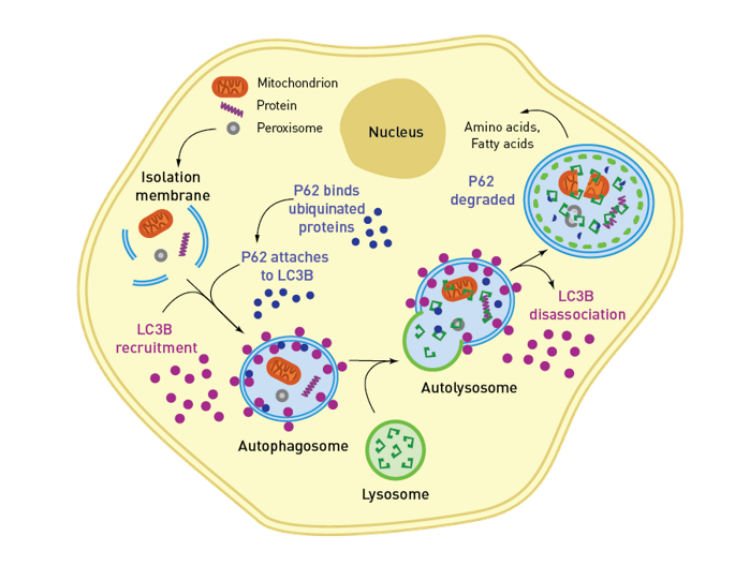
图1.LC3II-p62介导自噬模型
本实验拟利用人永生化角质形成细胞等构建实验模型,通过检测LC3II和P62蛋白表达,评价样品是否具有促进细胞自噬作用。
2、检测项目
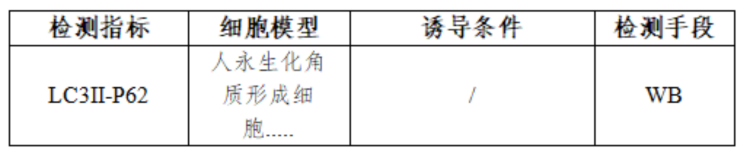
3.检测流程

4.部分结果展示

图1.LC3II/β-Actin比值柱形图
与正常对照组比,*p<0.05
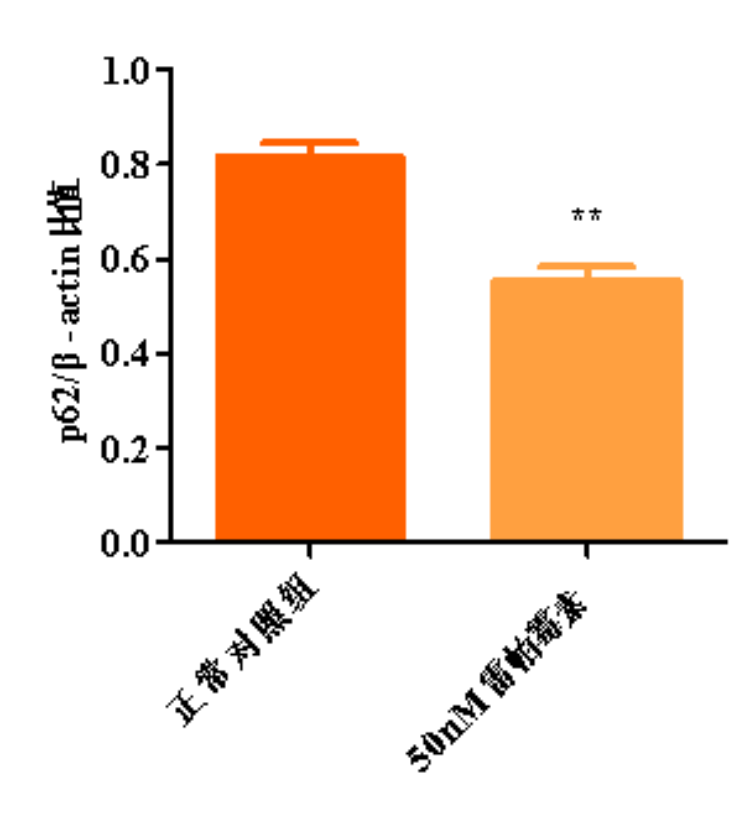
图2.p62/β-Actin比值柱形图
与正常对照组比,**p<0.01
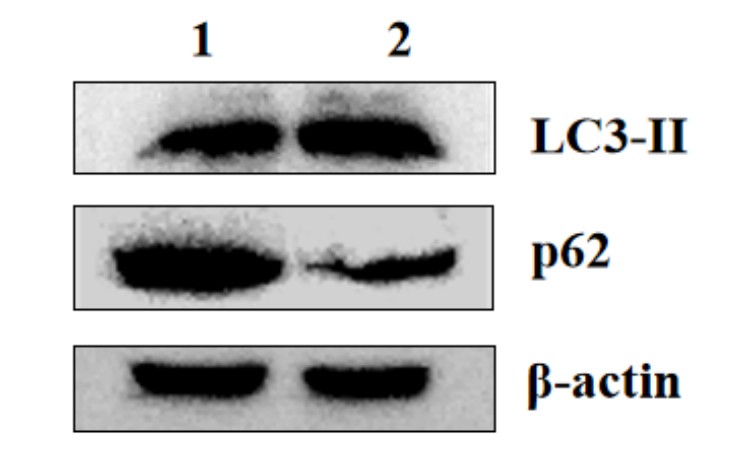
图3.LC3II,p62,β-Actin典型图
5.结果描述
根据测试结果,与正常对照组比,阳性对照组的LC3II/β-Actin比值显著上调,p62/β-Actin比值显著下调,说明本实验有效且可靠。
6.参考文献
[1]徐云云.自噬标记蛋白(Beclin1、LC3、p62、mTOR)在恶性肺结节中的表达及临床意义[D].西北民族大学,2021.
[2]隋馨莹,徐平,段昌柱,等.p62蛋白的分子功能及其在疾病中的研究进展[J].生物工程学报,2023,39(04):1374-1389.
[3]张翠.特发性膜性肾病肾组织中自噬相关蛋白LC3Ⅱ、P62和p-mTOR的表达及临床意义[D].蚌埠医学院,2022.
[4]李志元,张欣.细胞自噬研究方法的比较与分析[J].生物学杂志, 2018, 35(04):1-6.
[5]Li W, He P, Huang Y, Li YF, Lu J, Li M, Kurihara H, Luo Z, Meng T, Onishi M, Ma C, Jiang L, Hu Y, Gong Q, Zhu D, Xu Y, Liu R, Liu L, Yi C, Zhu Y, Ma N, Okamoto K, Xie Z, Liu J, He RR, Feng D. Selective autophagy of intracellular organelles: recent research advances. Theranostics. 2021 Jan 1;11(1):222-256.
[6]Miller DR, Thorburn A. Autophagy and organelle homeostasis in cancer. Dev Cell. 2021 Apr 5;56(7):906-918.
[7]Levine B, Kroemer G. Biological Functions of Autophagy Genes: A Disease Perspective. Cell. 2019 Jan 10;176(1-2):11-42.
[8]Klionsky DJ, Petroni G, Amaravadi RK, et al. Autophagy in major human diseases. EMBO J. 2021 Oct 1;40(19):e108863.
[9]Debnath J, Gammoh N, Ryan KM. Autophagy and autophagy-related pathways in cancer. Nat Rev Mol Cell Biol. 2023 Aug;24(8):560-575.
[10]Liu S, Yao S, Yang H, Liu S, Wang Y. Autophagy: Regulator of cell death. Cell Death Dis. 2023 Oct 4;14(10):648.
[11]Jeong SJ, Zhang X, Rodriguez-Velez A, Evans TD, Razani B. p62/SQSTM1 and Selective Autophagy in Cardiometabolic Diseases. Antioxid Redox Signal. 2019 Aug 20;31(6):458-471.
[12]Nagar R. Autophagy: A brief overview in perspective of dermatology. Indian J Dermatol Venereol Leprol. 2017, 83(3):290-297.
[13]Runwal G, Stamatakou E, Siddiqi FH, et al. LC3-positive structures are prominent in autophagy-deficient cells. Sci Rep. 2019 Jul 12;9(1):10147.
严正声明:以上内容所涉及的核心知识产权归杭州环特生物科技股份有限公司所有。任意第三方机构或个人在未经授权的前提下抄袭、剽窃、恶意传播均属侵害我司正当权益的行为,我司不排除诉诸一切法律手段维护自身合法权益。