业务咨询
![]() 发布时间:2024-01-15
发布时间:2024-01-15
![]() 环特生物
环特生物
![]() 浏览次数:3781
浏览次数:3781
上期我们介绍了保健品新规《目录》的 24 种保健功能声称。那么对于有市场需求,却不在《目录》中的保健功能,如国人热衷的“有益于关节健康”、“有益于围绝经期女性健康”、“有益于前列腺健康”等功能性声称产品该如何上市呢?
2023年8月,国家市场监管总局发布了《保健食品新功能及产品技术评价实施细则(试行)》(以下简称《实施细则》),引发行业高度关注。今天我们就结合《实施细则》进行要点解读。
解读一:开放式保健食品功能声称管理
《实施细则》明确提出任何单位或者个人在开展相关研究的基础上,可以单独或联合向国家市场监督管理总局食品审评中心(以下简称食品审评中心)提出新功能建议。对于不在《目录》中列出的保健功能声称,仍有机会获批。《实施细则》详细说明了新功能申报的流程、所需资料和试验要求等,这对于确保新功能的申报工作及保健品新功能的研发具有重要意义。
解读二:保健食品新功能定位明确,机理及其依据分类而定
随着产业不断成熟,细分市场、细分方向具有更多的机会。企业产品功能定位细分,也能更好地符合市场需要,同时也让产品的卖点具体化,从而打动消费者。
借鉴国际上功能性食品管理制度,新功能定位应当明确,分为补充膳食营养物质、维持或改善机体健康状况、降低疾病发生风险因素三类。并分类提出了相应的保健功能机理、依据和审查要求。

图注:保健食品新功能分类
解读三:保健食品新功能创新实行分级标注、动态管理
对应的新功能保健食品关联审评结论为“建议予以注册”的,食品审评中心根据保健功能科学依据的充足程度及国际上同类产品上市情况,分级标注保健食品新功能声称的限定用语。
上市后评价可依据评价结果动态调整功能声称的限定用语。新功能保健食品上市后评价后,依据科学共识充足程度对保健食品功能声称实行动态管理,可依据评价结果调整保健功能声称限定用语,用科学监管理念促进产业高质量发展。也就是说,某款新功能保健食品如果上市后评价良好,C级功能声称也可以调整为B级功能声称,甚至A级功能声称。

图注:分级标注保健食品新功能声称
解读四:关联审查保健食品新功能建议和新产品注册
《实施细则》规定,任何单位或者个人(以下简称建议人)同步提出新功能建议和对应的新功能保健食品注册申请的,在资料接收、审评、审批等各环节实行关联审查,以制度创新鼓励行业创新,激发产业创新内生动力,促进科研成果向产品上市的快速转化。
因此,除了保健食品新功能所涉及的试验项目外,还需要根据保健食品注册管理相关规定对新功能保健食品开展卫生学、毒理学试验等多项试验。
新功能建议纳入允许保健食品声称的保健功能目录(以下简称保健功能目录),应当通过新功能研究和技术评价,并对新功能保健食品开展上市后评价。
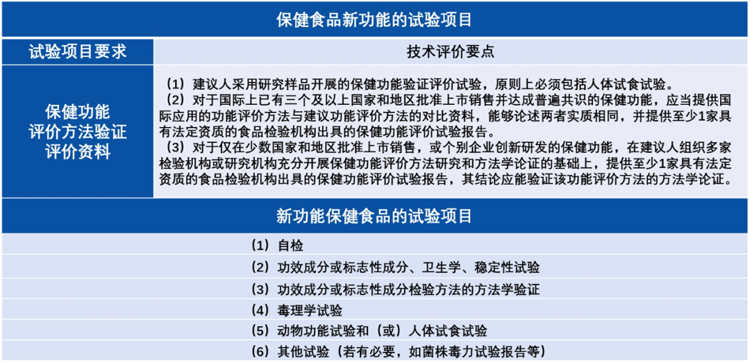
图注:保健食品新功能的试验项目
解读五:新功能评价方法必须包括人体试食试验
保健食品新功能产品实行上市前审评和上市后评价相结合,新功能评价方法原则上必须包括人体试食试验,是保健食品监管制度上的重大变革。
《实施细则》要求,评价指标及判定标准应科学、明确、可行,并经过验证评价。同时,验证评价应当充分评估实验室间差异,在提出新功能建议前,应当通过符合要求的至少1家食品检验机构或临床试验机构验证评价;同步提出新功能保健食品注册的,在上市后评价期间,应当通过符合要求的至少2家食品检验机构或临床试验机构验证评价。
解读六:上市前审评和上市后评价相结合的监管体系
由于保健食品对于人体的健康效应的显现需要较长时间实现,注册前基于动物实验和小样本量的人体试食试验的功能评价很难准确地诠释保健食品的完整科学内涵,需要逐步构建“事前审查”和“事后评价”相结合监管体系,为完善保健功能管理要求夯实科学依据基础。
上市后评价:注册证书有效期届满(6个月)前,新功能保健食品上市后评价符合要求,需对功能目录和保健食品功能声称限定用语等相关内容进行调整的,食品审评中心将调整建议等相关材料报送国家市场监督管理总局。符合要求的,按程序调整。
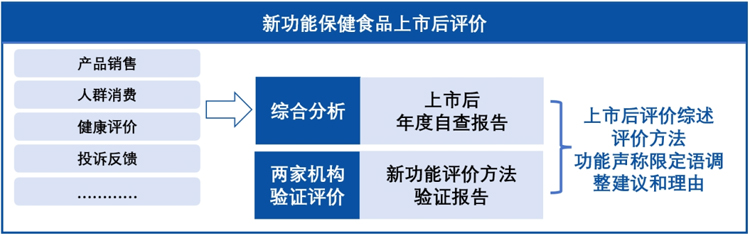
图注:新功能保健食品上市后评价
新功能申报“解锁”开启科研竞赛新时代
保健食品的新功能突破一直是行业高度关注的议题,《实施细则》的发布,是以制度创新引领产业创新,将为企业研发创新带来发展新机遇,加速行业整体创新的步伐。新功能申报技术壁垒较高,具备技术优势和产品研发优势的企业将在新功能赛道更具竞争力。
环特生物与多家具备注册或备案验证评价工作法定资质机构开展深度合作,可为各类保健功能食品的申报提供丰富的人体试食试验方案。同时,还提供集斑马鱼生物技术、哺乳动物实验平台、基因编辑技术等多维生物技术为一体的全方位、一体化的安全性和功效研究体系,为健康美丽产业探索多元化CRO与科研服务新路径,助力保健食品创新研发与应用!
【技术咨询】17364531293(微信同号)


