业务咨询

![]() 发布时间:2026-02-28
发布时间:2026-02-28
![]() 环特生物
环特生物
![]() 浏览次数:968
浏览次数:968

罕见病,不止罕见!罕见病远超人们的想象:已知罕见病超过7000种,我国公布的罕见病目录中已纳入207种疾病,涉及遗传(超过150种)、免疫(如自身免疫性脑炎、系统性硬化症等10余种)及肿瘤相关疾病;全球约3亿罕见病患者,我国罕见病群体规模约2000万人……近年来,斑马鱼因其与人类基因同源性高达87%、胚胎通体透明、基因编辑效率高、繁殖力强且适合高通量筛选等独特优势,正在让罕见病研究突破想象的边界!
本期,我们介绍几种环特生物可以为客户提供的基于斑马鱼构建的常用罕见病模型,包括Werner综合征、先天性脊柱侧凸、Acrofacial Dysostosis–Cincinnati 综合征(辛辛那提型肢面发育不良,AFDCIN)、Dravet综合征(DS)等,为罕见病药物筛选、致病机制研究及基因治疗探索提供科学的评价工具及科学依据,助力罕见病精准诊断,让罕见被看见!欢迎有需要的客户垂询!
01、构建斑马鱼Werner综合征模型
Werner综合征(WS),是一种罕见的常染色体隐性遗传病,表现为加速衰老,但Wrn敲除小鼠无法重现患者表型,缺乏理想的脊椎动物模型。
通过建立高效的脊椎动物早衰模型——Werner综合征特征的斑马鱼突变体,利用该模型进行大规模化合物筛选,并在早衰模型、生理性衰老斑马鱼及人类细胞中验证,最后阐明有效药物延缓衰老的分子机制。
wrn基因突变体斑马鱼在幼鱼期就表现出与Werner综合征患者相似的早衰特征,可作为高效的抗衰药物筛选平台,并在此基础上从小规模筛选中发现抗癌药物sapanisertib具有延缓衰老的潜力。
研究方法及指标
1. 通过ENU诱变筛选,获得wrn基因突变体(第5外显子T→A突变,提前终止密码子);
2. 细胞衰老标志:SA-β-Gal染色、p21/p53表达检测;
3. DNA损伤:γH2AX免疫荧光;表观遗传改变;肠道屏障功能;炎症反应;内质网应激;生存曲线、游泳活动度追踪等。
示意图展示
参考文献:J. Ma,Y. Chen,J. Song,Q. Ruan,L. Li, & L. Luo, Establishment and application of a zebrafish model of Werner syndrome identifies sapanisertib as a potential antiaging drug, Proc. Natl. Acad. Sci. 2025
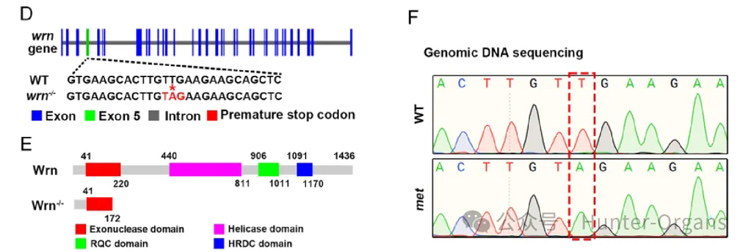
图1
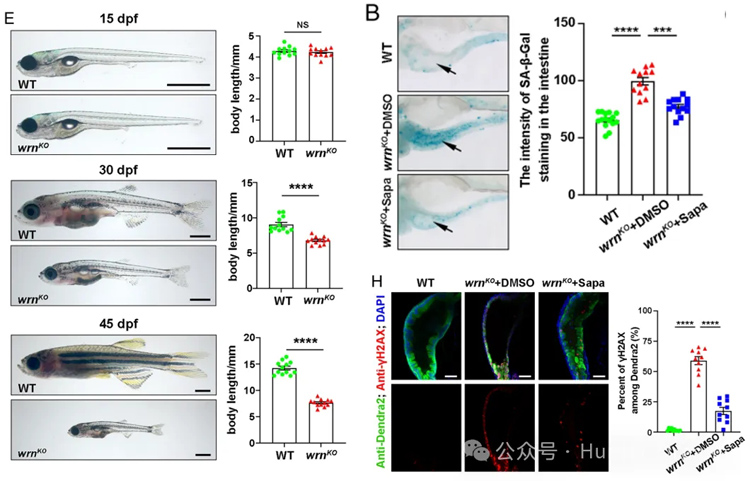
图2
02、构建斑马鱼先天性脊柱侧凸模型
先天性脊柱侧弯,也称先天性脊柱侧凸(Congenital Scoliosis,CS),是由于胚胎在发育期间受各种原因(环境污染、基因突变、维生素缺乏、化学药物因素以及病毒感染等)的影响,导致脊柱发育异常引起的脊柱畸形。
先天性脊柱侧弯的发病率在活产婴儿中约为(0.5~1)/1000,会影响婴幼儿及青少年的骨骼发育,使身体变形,出现驼背、身材矮小扭曲的现象,严重者还可能影响心肺功能、肾脏功能、肠胃系统,心理等,甚至累及脊髓神经造成瘫痪。已发现Notch信号通路等多个基因突变可导致CS,但大多数家族性或散发性病例的遗传原因仍未知。
通过ENU化学诱变筛选,鉴定导致先天性脊柱侧凸样椎体畸形的基因;解析分子机制,阐明该基因在脊柱发育中的具体作用机制,揭示该基因调控的下游信号通路及其与疾病的关系。
研究结果显示,dstyk突变导致CS样表型,突变体鱼脊索液泡生物发生缺陷,导致轴骨分割模式破坏,成年期严重脊柱侧凸和驼背、椎体畸形。脊索液泡是特化的溶酶体相关细胞器(LROs),Dstyk通过mTORC1/TFEB通路调控溶酶体/液泡生物发生。mTORC1抑制剂Torin1可部分rescue突变体表型,提示mTOR通路为潜在治疗靶点。
研究方法及指标
1. 通过ENU诱变筛选,观察体节缩短和脊柱弯曲表型,获得smt(somite shorten)突变系,并定位到22号染色体dstyk基因;
2. 通过转基因品系和活细胞成像、X-ray、micro-CT等连续观察突变体鱼脊索建立过程。
示意图展示
参考文献:Sun, X., Zhou, Y., Zhang, R. et al. Dstyk mutation leads to congenital scoliosis-like vertebral malformations in zebrafish via dysregulated mTORC1/TFEB pathway. Nat Commun 11, 479 (2020)
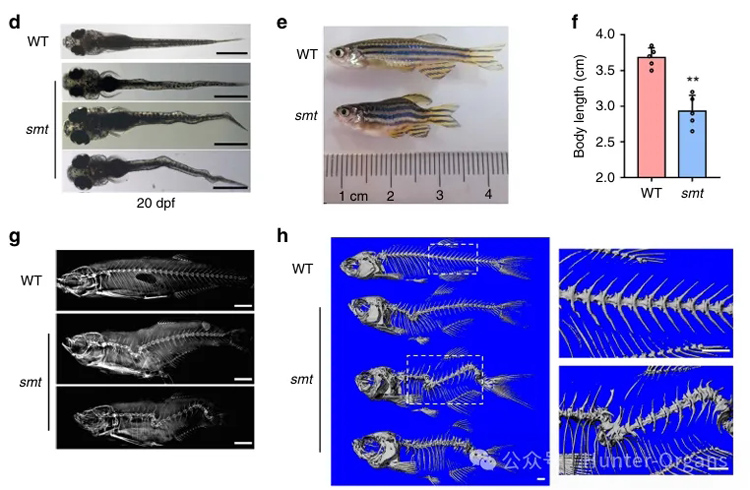
图3
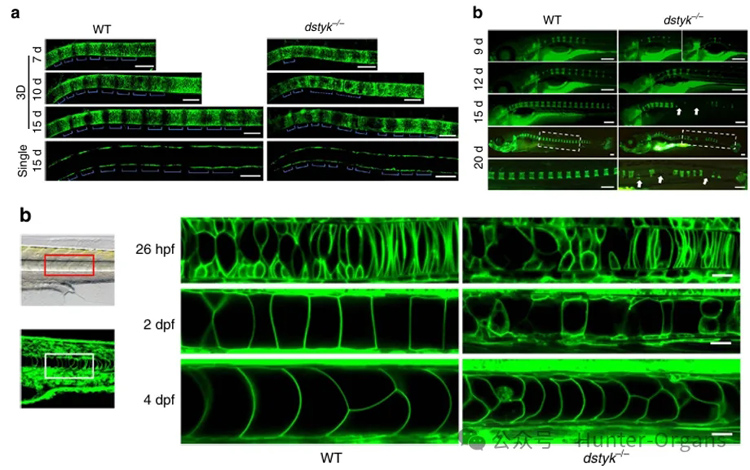
图4
03、斑马鱼模型在AFDCIN综合征中的应用
Acrofacial Dysostosis–Cincinnati 综合征(辛辛那提型肢面发育不良,AFDCIN)是一种罕见的先天性颅面和肢体骨骼发育异常综合征,表现为颌面发育不良和肢体畸形。该疾病由 POLR1A 基因的致病变异引起,POLR1A 编码 RNA 聚合酶 I 的最大亚基,参与核糖体 RNA 的转录。
通过斑马鱼模型,研究 POLR1A 基因突变如何影响核糖体生物合成,进而导致颅面和肢体骨骼发育异常。研究 Tp53 信号通路在 AFDCIN 发病机制中的具体贡献,并探索是否存在Tp53独立的机制。
在 polr1a–/– 突变体中,Tp53 依赖的细胞凋亡是导致颅面骨骼发育不良的重要机制。通过遗传抑制 Tp53(生成 polr1a–/–; tp53–/– 双突变体),可以部分改善早期胚胎发育中的细胞凋亡和颅面骨骼发育不良,但无法完全恢复。
研究方法
通过基因编辑技术构建 POLR1A 基因敲除突变体(polr1a–/–)、 Tp53 突变体(tp53–/–) ,并生成双突变体(polr1a–/–; tp53–/–)。
示意图展示
参考文献:Watt KEN, Neben CL, Hall S, et al. tp53-dependent and independent signaling underlies the pathogenesis and possible prevention of Acrofacial Dysostosis–Cincinnati type. Hum Mol Genet. 2018
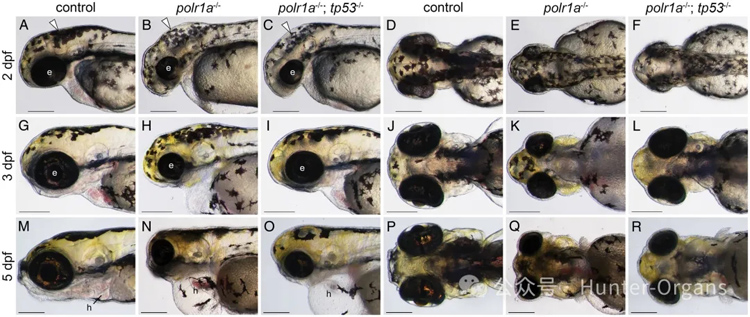
图5
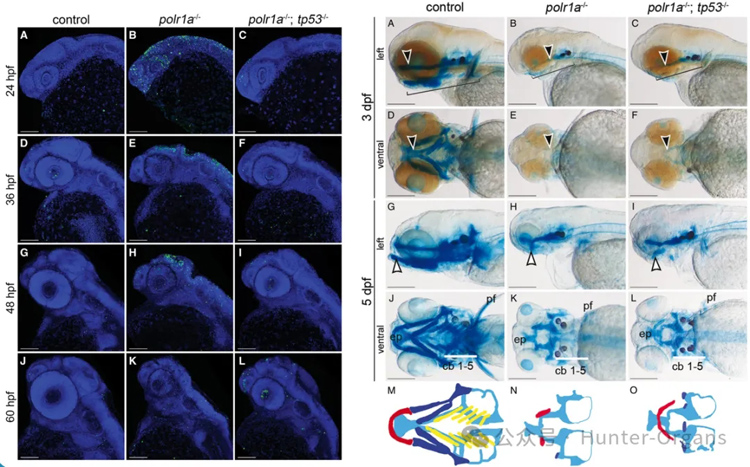
图6
04、斑马鱼模型在婴儿严重肌阵挛性癫痫中的应用
Dravet综合征(DS)是一种由SCN1A基因突变引起的严重儿童期癫痫,其特征包括智力障碍、社交发展受损和持续的药物难治性癫痫发作。SCN1A基因编码的Nav1.1是一种电压门控钠通道,其突变与DS的发生密切相关。目前,DS的治疗选择有限,且大多数抗癫痫药物(AEDs)对DS患者的疗效不佳。
通过斑马鱼模型,筛选能够改善DS相关癫痫表型的化合物,以期发现新的治疗DS的药物。scn1Lab突变体斑马鱼表现出与DS患者相似的癫痫表型,包括自发的癫痫发作、过度活跃和惊厥行为。通过高通量药物筛选,研究团队发现克列咪唑(clemizole)能够显著抑制scn1Lab突变体的癫痫发作行为和电图癫痫活动。
研究方法
1. 利用化学诱变筛选得到了SCN1A基因突变的斑马鱼(scn1Lab),这些突变体表现出自发的异常电图活动、过度活跃和惊厥行为;
2. 设计了一个高通量药物筛选策略,通过监测斑马鱼的游泳行为和电图活动,筛选能够抑制突变体癫痫发作的化合物。
结果展示
参考文献:Baraban SC, Dinday MT, Hortopan GA. Drug screening in Scn1a zebrafish mutant identifies clemizole as a potential Dravet syndrome treatment. Nat Commun. 2013;4:2410.
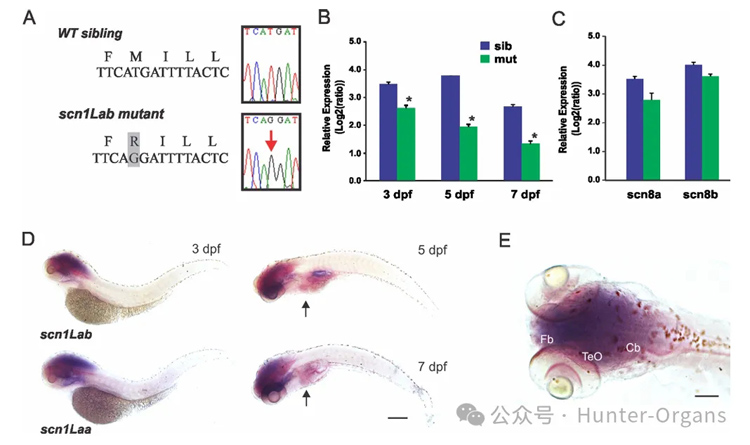
图7
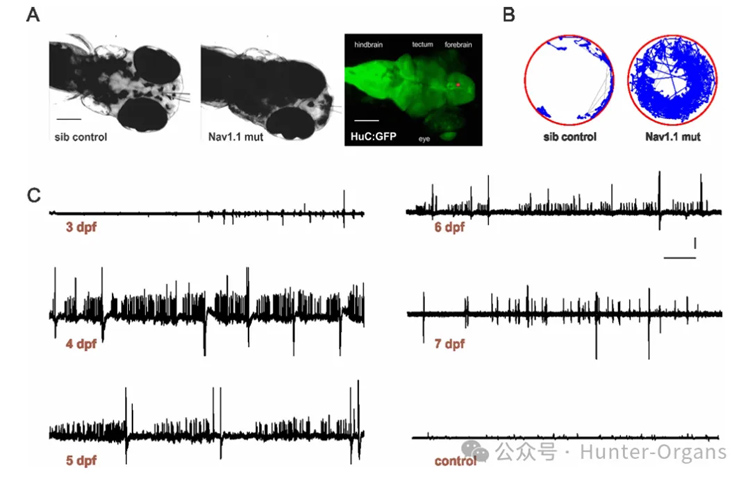
图8